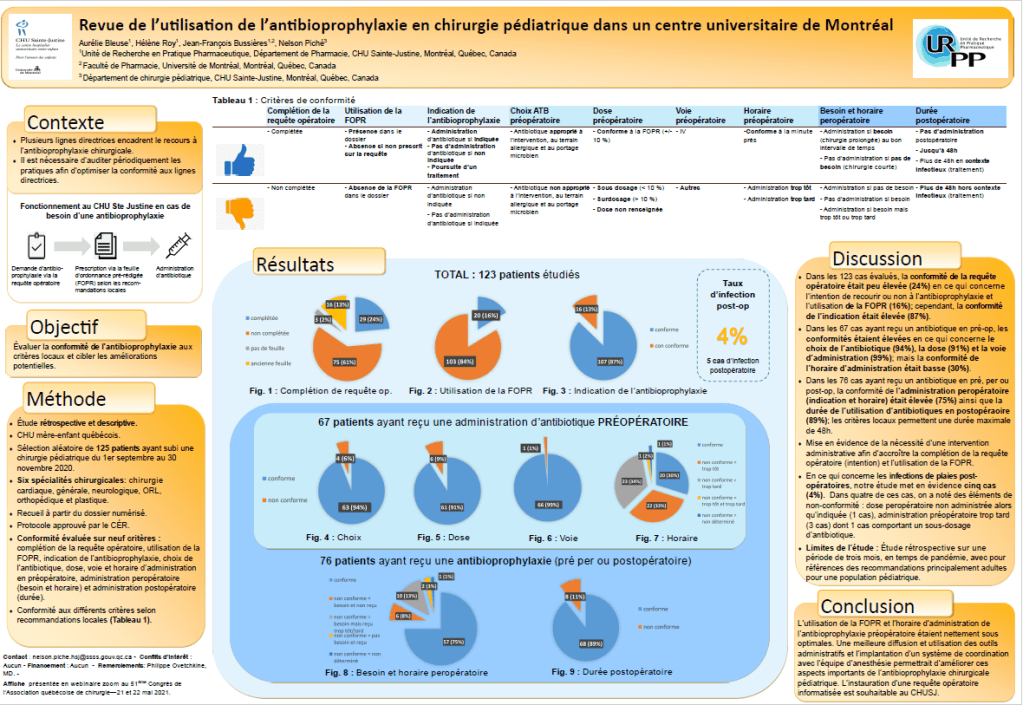
Plusieurs lignes directrices encadrent le recours à l’antibioprophylaxie chirurgicale. Il est donc nécessaire d’auditer périodiquement les pratiques afin d’optimiser la conformité aux lignes directrices.
Une étude rétrospective et descriptive a été menée au CHU Sainte-Justine de Montréal afin d’évaluer la conformité de l’antibioprophylaxie aux critères locaux et cibler les améliorations potentielles.
Pour cela, 125 patients ayant subi une chirurgie pédiatrique du 1er septembre au 30 novembre 2020 ont été sélectionnés. Les données ont été recueillies à partir du dossier numérisé pour 6 spécialités chirurgicales. La conformité a été évaluée sur neuf critères : complétion de la requête opératoire, utilisation de la FOPR, indication de l’antibioprophylaxie, choix de l’antibiotique, dose, voie et horaire d’administration en préopératoire, administration peropératoire (besoin et horaire) et administration postopératoire (durée).
Il a été retrouvé que dans les 123 cas évalués, la conformité de la requête opératoire en ce qui concerne l’intention de recourir ou non à l’antibioprophylaxie (24%) et l’utilisation de la FOPR (16%) était peu élevée. Cependant, la conformité de l’indication (87%) était élevée. En ce qui concerne les infections de plaies post-opératoires, l’étude met en évidence cinq cas (4%). Dans quatre de ces cas, on a noté des éléments de non-conformité.
Finalement, l’utilisation de la FOPR et l’horaire d’administration de l’antibioprophylaxie préopératoire étaient nettement sous optimales. Une meilleure diffusion et utilisation des outils administratifs et l’implantation d’un système de coordination avec l’équipe d’anesthésie permettrait d’améliorer ces aspects importants de l’antibioprophylaxie chirurgicale pédiatrique.
Vous pouvez consulter notre article publié dans les Annales Pharmaceutiques Françaises et notre affiche présentée au 51ème Congrès de l’Association québécoise de chirurgie le 21 mai 2021.










Vous devez être connecté pour poster un commentaire.