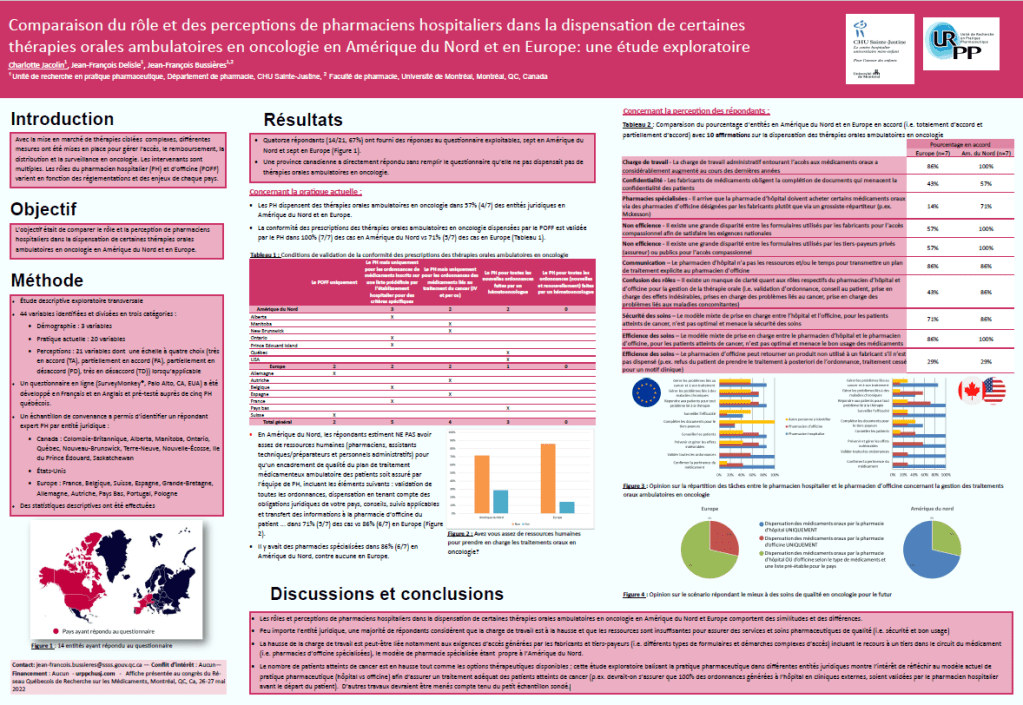
Avec la mise en marché de thérapies ciblées complexes, différentes mesures ont été mises en place pour gérer l’accès, le remboursement, la distribution et la surveillance en oncologie. Les intervenants sont multiples. Les rôles du pharmacien hospitalier (PH) et d’officine (POFF) varient en fonction des réglementations et des enjeux de chaque pays.
Une étude descriptive exploratoire transversale a été menée afin de comparer le rôle et la perception des pharmaciens hospitaliers dans la dispensation de certaines thérapies orales ambulatoires en oncologie en Amérique du Nord et en Europe.
Pour cela, 44 variables identifiées et divisées en trois catégories (démographie, pratique actuelle et perceptions). Un questionnaire en ligne (SurveyMonkey®, Palo Alto, CA, EUA) a été développé en Français et en Anglais et pré-testé auprès de cinq PH québécois. Un échantillon de convenance a permis d’identifier un répondant expert PH par entité juridique (Canada, États-Unis et Europe). Des statistiques descriptives ont ensuite été effectuées.
Il a été retrouvé que les rôles et perceptions de pharmaciens hospitaliers dans la dispensation de certaines thérapies orales ambulatoires en oncologie en Amérique du Nord et Europe comportent des similitudes et des différences. Peu importe l’entité juridique, une majorité de répondants considèrent que la charge de travail est à la hausse et que les ressources sont insuffisantes pour assurer des services et soins pharmaceutiques de qualité (i.e. sécurité et bon usage). La hausse de la charge de travail est peut-être liée notamment aux exigences d’accès générées par les fabricants et tiers-payeurs (i.e. différents types de formulaires et démarches complexes d’accès) incluant le recours à un tiers dans le circuit du médicament (i.e. pharmacies d’officine spécialisées), le modèle de pharmacie spécialisée étant propre à l’Amérique du Nord. Le nombre de patients atteints de cancer est en hausse tout comme les options thérapeutiques disponibles ; cette étude exploratoire balisant la pratique pharmaceutique dans différentes entités juridiques montre l’intérêt de réfléchir au modèle actuel de pratique pharmaceutique (hôpital vs officine) afin d’assurer un traitement adéquat des patients atteints de cancer (p.ex. devrait-on s’assurer que 100% des ordonnances générées à l’hôpital en cliniques externes, soient validées par le pharmacien hospitalier avant le départ du patient). D’autres travaux devraient être menés compte tenu du petit échantillon sondé.
Vous pouvez consulter notre affiche présentée au Grand Forum 2021 de l’Association des pharmaciens des établissements de santé du Québec (A.P.E.S.) le 25 mars 2021.

Vous devez être connecté pour poster un commentaire.