Les changements apportés à la Loi sur les aliments et drogues en 2019 obligent la déclaration des réactions indésirables aux médicaments (RIM) graves par les établissements de santé au Canada. Au Québec, le Ministère de la Santé et des Services sociaux a implanté en 2023 le financement à l’activité. L’impact économique des RIM en établissements de santé reste méconnu.
Une revue de la littérature a donc été réalisée afin de décrire les coûts associés à la survenue de RIM.
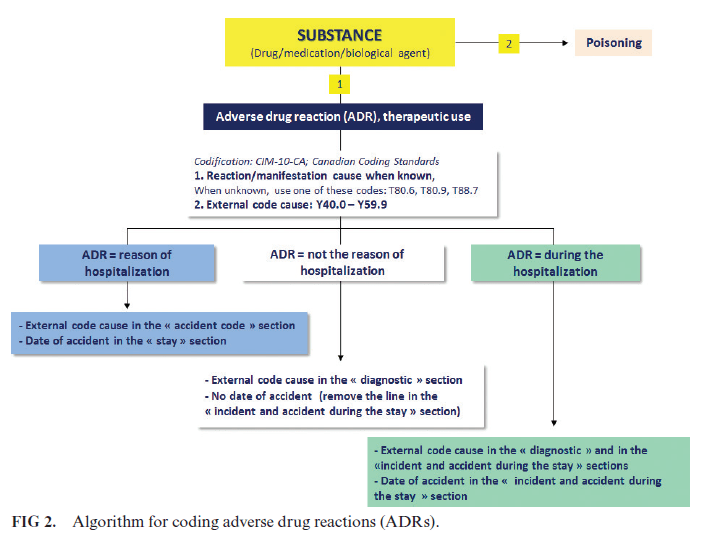
Pour cela, une recherche a été menée dans la base de données PubMed pour recenser les articles publiés entre le 1er janvier 2017 et le 31 décembre 2021, relatifs à ce sujet. Les données concernant le pays, la perspective économique, la RIM, les médicaments et les coûts ont été collectées.
Les résultats ont montré que les RIM engendrent des coûts additionnels, mais pas forcément dans
tous les cas. Les données économiques associées aux RIM sont hétérogènes et ne peuvent être appliquées directement aux contextes québécois et canadien. Des travaux locaux sont nécessaires afin de quantifier les coûts associés aux RIM en établissements de santé au Canada.
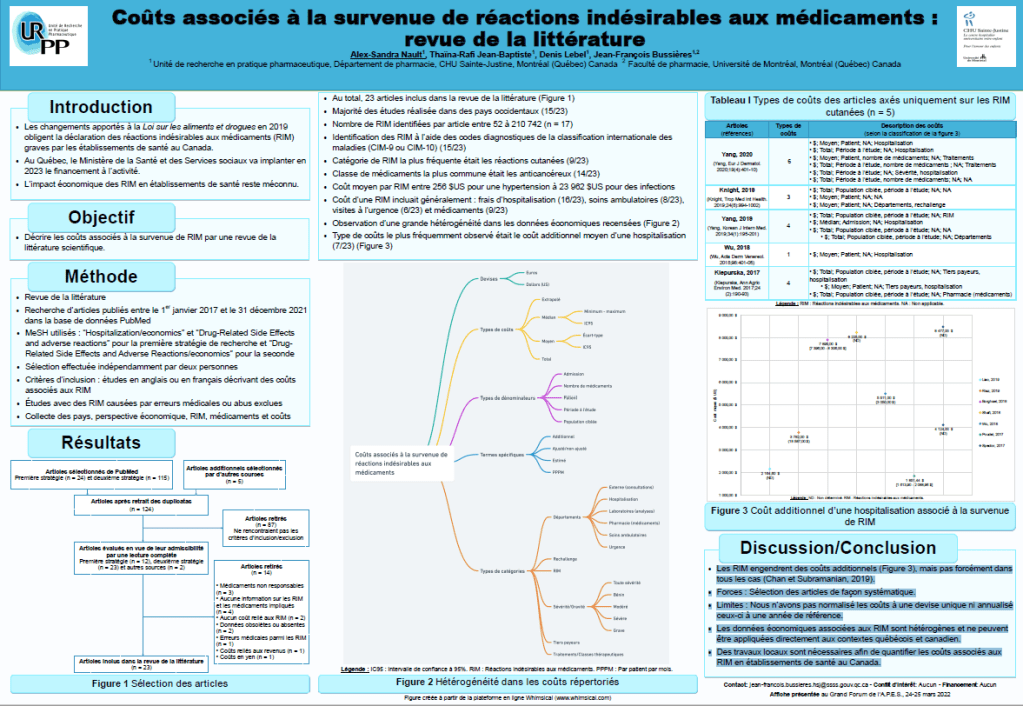
Vous pouvez consulter notre affiche présentée au Grand Forum 2022 de l’Association des pharmaciens des établissements de santé du Québec (A.P.E.S.) le 25 mars 2022.





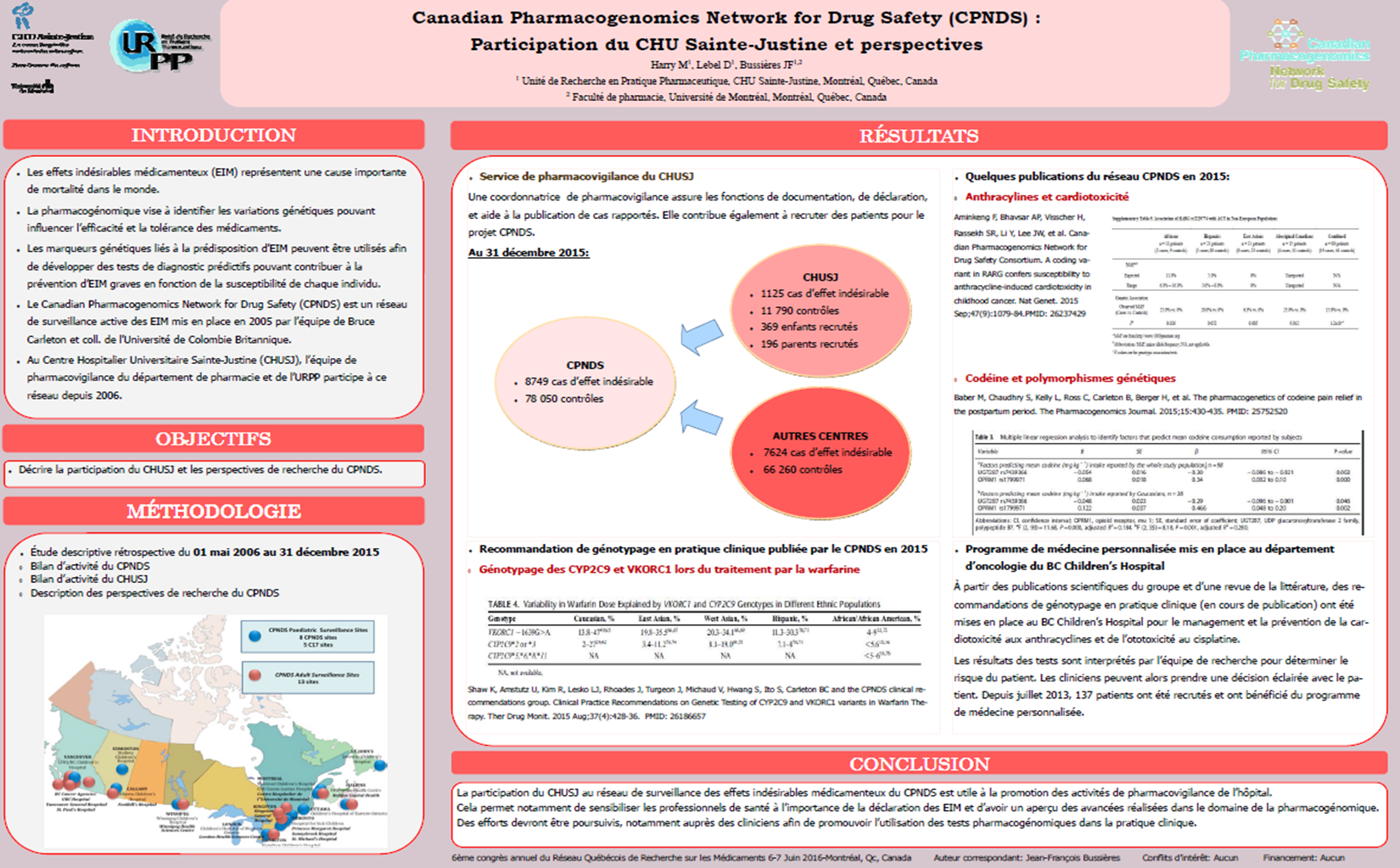


Vous devez être connecté pour poster un commentaire.