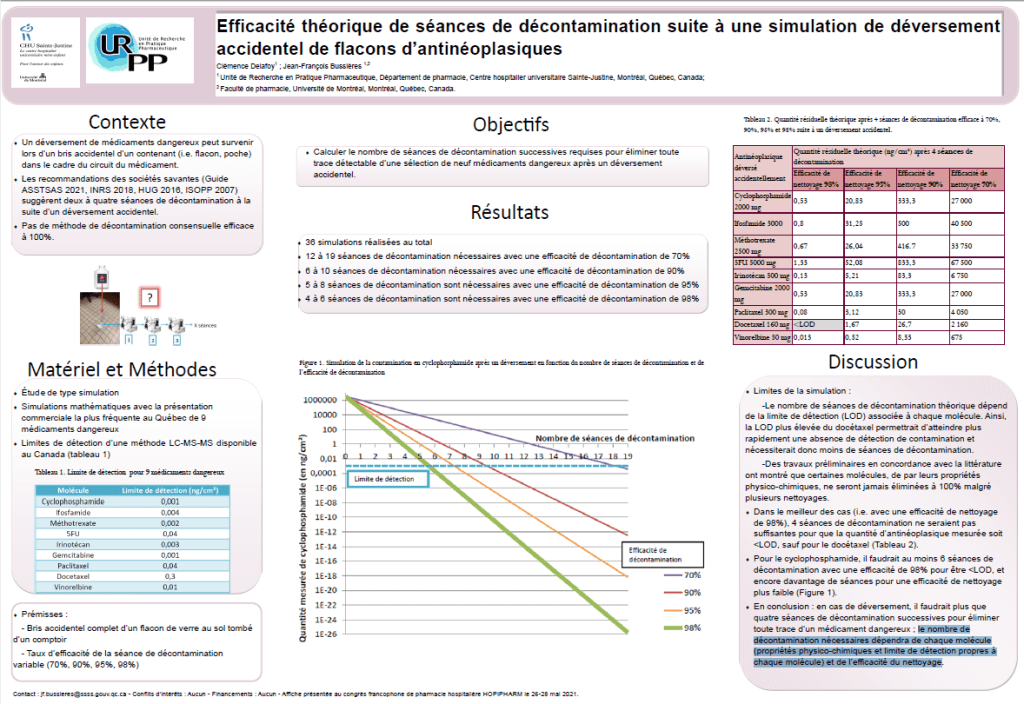
Des difficultés à décontaminer complètement les surfaces exposées aux antinéoplasiques existent. Il est nécessaire d’effectuer plusieurs nettoyages successifs. Malgré cela, le cyclophosphamide, très utilisé, est persistant sur les surfaces. C’est pourquoi le protocole de décontamination a été amélioré entre 2020 et 2021.
Une étude a été réalisée afin d’évaluer l’efficacité d’un protocole de décontamination en huit étapes et ses effets après 30 jours sur la contamination environnementale par le cyclophosphamide. Il était également question de comparer deux protocoles de décontamination (2020 en quatre étapes vs 2021 en huit étapes)
La contamination par le cyclophosphamide a été quantifié à T0, T1 et T2. La mesure s’est faite par chromatographie liquide haute performance couplée à la spectrométrie de masse. L’étude a été réalisée dans 9 pharmacies hospitalières au Québec. 17 sites on été sélectionnés dont les grilles frontales et planchers de hottes et les tablettes d’entreposage du cyclophosphamide.
Il a été retrouvé que le nettoyage intensif n’a pas permis d’enlever toutes les traces de cyclophosphamide même s’il y avait une diminution de la contamination juste après le nettoyage. De plus, une ré-augmentation de la contamination après 30 jours de travail avait lieu. Au sujet de la comparaison des protocoles, il y avait une diminution du nombre de sites contaminés entre 2020 et 2021 pour T0 et T1. Toutefois, une même proportion des sites était contaminée après 30 jours de travail.

Vous pouvez consulter notre article publié dans la revue Objectif Prévention et notre affiche présentée au Réseau québécois de recherche sur les médicaments (RQRM) le 10 juin 2021.








Vous devez être connecté pour poster un commentaire.